آنالیز ولتامتری از مهمترین روش های مطالعه خواص خوردگی مواد است. این آزمون از دو روش، ولتامتری چرخه ای و خطی تشکیل شده است. اساس روش پلاریزاسیون است. به غیر از مطالعه رفتار خوردگی مواد، از این روش ها در کاربردهای زیستی مانند سنجش میزان مولکول ها استفاده می شود. در این مقاله هر دو روش ولتامتری خطی (LSV) و ولتامتری چرخه ای (CV) شرح داده شده اند. در این مقاله با تئوری این دو روش و چگونگی تحلیل آنها نیز آشنا می شوید.
آزمون ولتامتری یکی از روش های آنالیز و پایش پرکاربرد خوردگی مواد گوناگون می باشد. این آزمون در دو نوع ولتامتری چرخه ای و خطی انجام می گیرد. در این روش ها از الکترود جامد، به عنوان الکترود کار استفاده می شود. این الکترود هم جنس با ماده ای می باشد که قرار است آنالیز شود. اساس کار این روش پلاریزاسیون میباشد. پلاریزاسیون اصطلاحی به معنای افزایش یا کاهش پتانسیل الکترود در اثر عبور جریان از آن است .از این روش برای مطالعه فرایند های ردوکس، تشخیص پایداری نمونه در یک واکنش، برگشت پذیری واکنش، تعیین ضریب نفوذ و سرعت انتقال الکترون استفاده می شود. بررسی انواع خوردگی های صورت گرفته در آلیاژها توسط این روش انجام می گیرد. آزمون ولتامتری روش حساس تری نسبت به سایر روش ها است. از مزیت دیگر این روش آن است که امکان اندازه گیری ترکیبات آلی مانند آلدهید ها، کتون ها، آلکن ها و ترکیبات آروماتیک وجود دارد. این روش همچنین توانایی اندازه گیری غلظت های خیلی کم در حد ppm و گاهی نیز در حد ppb را دارد.
جریان حد متناسب با غلظت آنالیت می باشد. در ولتامتری عامل تعیین کننده مقدار جریان حد، نفوذ است، و همچنین فرایند انتقال جرم توسط نفوذ انجام می شود. جریان حد از رابطه زیر قابل محاسبه است.
Ilim = (ηFDAc) / d
که در آن η اضافه ولتاژ یا پلاریزاسیون غلظتی، F عدد فاراده، D ضریب نفوذ آنالیت، A مساحت سطح الکترود، c غلظت مولار آنالیت و d ضخامت لایه تحت تاثیر نفوذ می باشد. بنابراین عوامل تعیین کننده حدI، ضریب نفوذ آنالیت و غلظت آنالیت می باشند.
آزمون ولتامتری خطی (LSV)
آنالیز LSV از روش های ولتامتری است که کاربرد های گوناگونی در صنایع مختلف دارد. این آزمون براساس اعمال پتانسیل به سیستم و سپس اندازه گیری جریان انجام می شود. اختلاف پتانسیل بین یک الکترود مرجع و الکترود کار (WE) اعمال می شود. پس از اعمال اختلاف پتانسیل بین دو الکترود نموداری توسط دستگاه رسم می شود که به آن ولتاموگرام گفته میشود. نمودار رسم شده می تواند جریان برحسب ولتاژ یا ولتاژ برحسب جریان باشد. با استفاده از این نمودار شاخه آندی و کاتدی مشخص می شود. شیب هر کدام از شاخه ها را در ناحیه خطی رسم می شود و از تقاطع شیب های اندازه گیری شده می توان جریان خوردگی را بدست آورد. سپس از جریان خوردگی به میزان خوردگی پی می برند. در شکل های ۱ و ۲ نمونه هایی از نمودار های ولتاموگرام قابل مشاهده است. شکل ۱ نیز شکل دیگری از ولتاموگرام را نمایش میدهد که تاثیر سرعت تغییر پتانسیل بر تغییرات جریان نمایش داده شده است. هر چه سرعت پویش بیشتر شود تغییرات جریان بیشتر و شدیدتر می باشد.
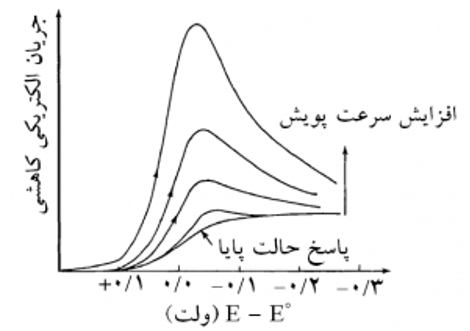
شکل ۱- ولتاموگرام روبش خطی برای واکنش کاهش در الکترود جامد به صورت تابعی از سرعت تغییر پتانسیل.
آزمون ولتامتری چرخهای (CV)
ولتامتری چرخهای یکی از روش ها در مطالعه واکنشهای الکتروشیمیایی انجام شده هنگام خوردگی است. این روش با استفاده از این واکنش ها می تواند بسیاری از مکانیزمهای خوردگی را تعیین کند. این روش بر اساس اعمال یک ولتاژ سیکلی کوچک با دامنه پایین انجام می گیرد. پتانسیل الکترود کار به صورت خطی با زمان تغییر داده می شود. بعد از رسیدن به یک پتانسیل تعیین شده، پتانسیل الکترود کار در جهت عکس تغییر میکند تا به پتانسیل اولیه بازگردد (در ولتامتری خطی تغییر در جهت عکس نداشتیم). چرخههای تغییر پتانسیل میتوانند به تعداد دلخواه تکرار و انجام شوند. جریان سیستم پارامتری است که اندازه گیری می شود. سپس نمودار ولتاژ بر حسب جریان رسم می شود. نمودار رسم شده حاوی پیک هایی می باشد که با اندازه گیری میزان جریان و پتانسیل در این پیک ها، می توان مکانیزمها و نوع واکنشهایی که در هنگام خوردگی صورت می گیرد را پیش بینی نمود. کاربرد مهم این روش برای سنسورهای الکتروشیمیایی جهت تعیین غلظت یک ماده و محاسبه نمودن پارامترهای فیزیکی مانند ضریب نفوذ و ضریب الکتیویته یک جزء در سیستم و محاسبه پارامترهای خوردگی مانند مقاومت پلاریزاسیون می باشد.
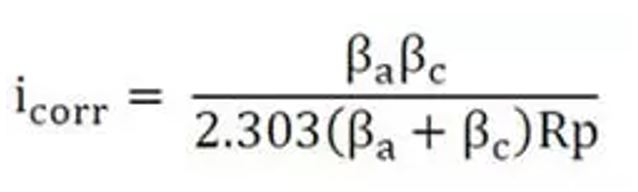
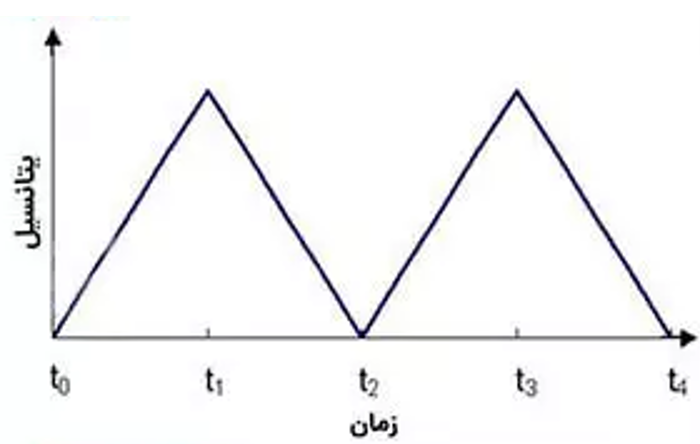
شکل ۳- اعمال ولتاژ متناوب.
تحلیل نمودار حاصل
اگر فرآیندهای انجام گرفته از لحلظ ترمودینامیکی برگشت پذیر باشند، پیک های تشکیل شده دارای اندازه و شکل مشابهی می باشند. میزان جریان با غلظت ماده ای که در حال اکسایش و کاهش است، ارتباط دارد. در صورتی که جریان رفت و برگشت یکی بود در پایان سیکل ماده احیا شده است. در سیکل برگشت، در صورتی که پتانسیل به حالت پتانسیل اولیه برگشت ولی مقدار کم جریان هنوز وجود داشت، نشان می دهد که بخشی از ماده مورد نظر کاهیده نشده است.
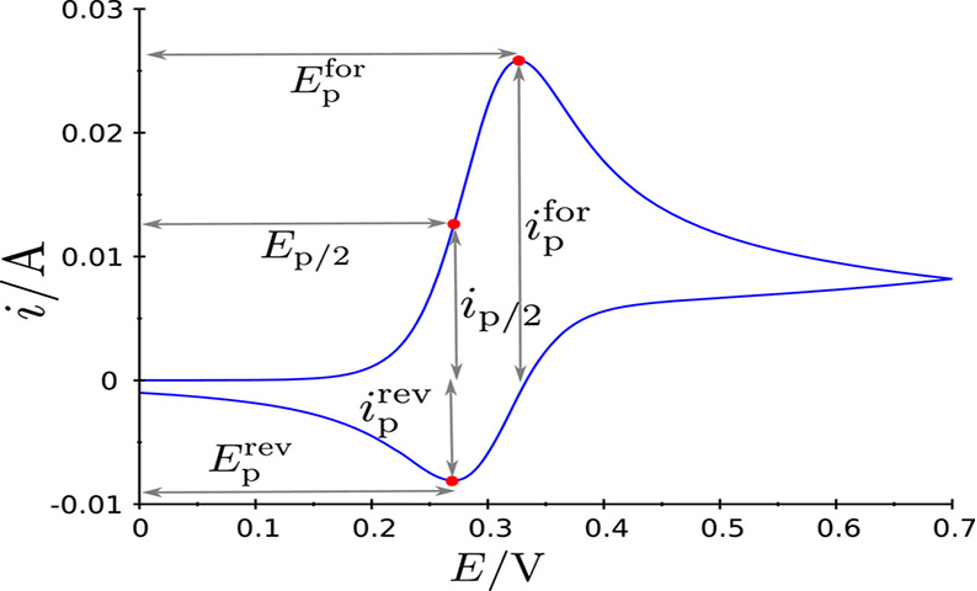
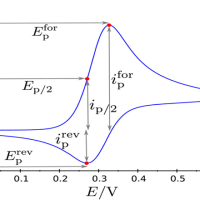
شکل ۴- طرح واره ای از ولتاموگرام چرخه ای برای واکنش کاهش در یک الکترود جامد.
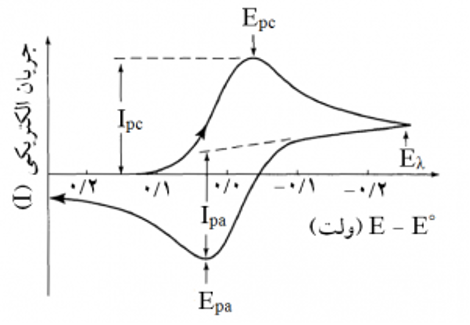
شکل ۵- طرح دیگری از نمودار حاصل.
انتخاب روش ولتامتری مناسب میتواند رفتار الکتروشیمیایی مواد مختلف را به خوبی ارزیابی کند. بررسی خوردگی در آلیاژها و تجزیه کیفی و کمی مواد آلی، داروها، یون های فلزی و ترکیبات بیوشیمیایی با دقت خوبی توسط این روش امکان پذیر می باشد.